★ Despre chimismul postminier la Roşia Montană (VI)
Identificarăm în episodul trecut o serie de substanţe ce rezultă în procesul de extracţie şi în cel de detoxifiere, din care, cea mai mare parte sunt insolubile, iar ionul cheie este cel de calciu provenit din milionul de tone de var nestins ce va fi folosit în cei 16 ani. Menţinerea pH-ului din lac la valori mari asigură precipitarea elementelor toxice, dar nu integrală. Am identificat o posibilă acumulare de seleniu (şi probabil şi de telur), în supernatant. Tot la extracţie rezultă şi mici cantităţi de hidrogen seleniat, un produs volatil. Cît este în uzină nu este nicio problemă. Gazele trec oricum printr-un scrubăr de spălare. E de asemeni foarte probabil ca seleniul să se oxideze în timpul procesului de detoxifiere, dar asta nu rezolvă problema, deoarece seleniţii şi seleniaţii sunt în majoritate solubili.
Arsenul, de asemeni, va mai ridica probleme pe termen scurt şi mediu, deoarece oxidarea şi polimerizarea lui nu au loc spontan. E foarte probabil ca de la detoxifiere, o mare parte din arsen să rămînă tot sub formă de sulfură. Care, la concentraţia de saturaţie de 40mg/l, depăşeşte de o mie de ori concentraţia maximă admisibilă.
Prezenţa unor solubile quasipermanente, chiar dacă la concentraţii mici, în iaz, obligă exploatatorul ca în perioada de operare să folosească apa de acolo doar în circuit închis. Aşa e şi prevăzut în proiect. Doar apele „bătrîne”, provenite de pe valea Roşia pot fi epurate în staţie, cu mai puţină bătaie de cap. Eventual trimise pe cele două văi, ca debit salubru. Şi acest lucru este prevăzut în documentaţie.
Să ne aplecăm acum asupra chimismului din iaz.
Am preluat dintr-un ziar schema de transformare:

Schema cuprinde transformările cianurilor în cele trei faze: gazoasă, lichidă, solidă. Să le luăm pe rînd:

Pe ramura din stînga sus este schematizată fotoliza acidului cianhidric. Ponderea reacţiei este extrem de mică, nu numai pentru că zilele senine sunt puţine iar nopţile senine nu contează, ci pentru că concentraţia iniţială este mică: 3mg/l la ieşirea din tulumbă. Dacă socotim 15 zile durata de recirculare totală a supernatantului şi a exfiltratului, rezultă o concentraţie medie de background de 1mg/l. La 1mg/l şi la pH=8, nu mai zboară practic nimic din acidul cianhidric. Pe ramura din dreapta este figurată degradarea biologică. Ea are loc în mediu aerob, la liziera iazului, la suprafaţa mîlurilor. Este practic hidroliza nitrilului la amoniac şi dioxid de carbon. Unele bacterii au darul să decarboxileze (să metabolizeze azotul şi să elibereze dioxidul de carbon) altele, să dezamineze (să metabolizeze carbonul şi să elibereze amoniacul. Cum amoniacul are solubilitate mare, nu este deloc exclus ca el să fie metabolizat direct de bacteriile iubitoare de azot. Fiind un proces aerob, amoniacul poate fi oxidat mai departe la azotiţi şi azotaţi. Însă ponderea procesului este relativ mică, datorită conţinutului mic de cianuri solubile. Nitriţii şi nitraţii sunt repede absorbiţi de către vegetaţia de plaur din vecinătate. Fenomenul se petrece în ape foarte puţin adînci, sau în sediment umed expus.
Aşadar, la interfaţa gaz-lichid şi în ape foarte puţin adînci, au loc procese oxidative.
Tot proces oxidativ întreţinut de către microorganisme este şi oxidarea arsenului la arseniţi şi mai ales la arseniaţi, precum şi cea a seleniului la seleniţi şi seleniaţi. Biosinteza arseniaţilor în prezenţa fierului şi a calciului*) dă naştere unor pelicule de arseniat de fier trivalent extraordinar de rezistente şi de impermeabile, ce îmbracă eventualele particule purtătoare de potenţiale surse de toxicitate metalică. Fenomenul de glazurare cu poliarseniaţi are loc în mod natural şi în haldele de pe valea Roşia, şi în galerii, dar mult mai dezordonat, cu eficacitate mult mai mică, din cauza acidităţii.
Este de la sine înţeles că, odată cu oxidarea seleniului are loc şi oxidarea la sulfaţi a sulfurilor rămase neatinse de procesul tehnologic.
Observăm că la biodegradarea oxidativă au loc atît fenomene dorite, cît şi fenomene nedorite. Unele substanţe precipită, altele devin solubile. Unele ies din sistem, altele precipită.
Continuăm. O altă serie de reacţii ce au loc în mediul apos este cea de fotoliză a complecşilor ciano-metalici:
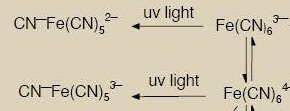
Trebuie spus că fotoliza complecşilor este valabilă în primii milimetri de apă sau în primul milimetru al nămolurilor expuse la soare. Deoarece complecşii înşişi ecranează pătrunderea luminii în stratele adînci. Ponderea fotolizei complecşilor metalici este mult mai mică în apă decît în mîluri. Dar odată eliberat acidul cianhidric, el însuşi se descompune fotochimic. Sau polimerizează. Fiind reacţii în mediul alcalin, este de aşteptat ca ionii centrali din complecşi să precipite sub forma hidroxizilor corespunzători.
Grosul metamorfozei are loc însă în adîncime, acolo unde se adună peste 90% din complecşii ciano-metalici. Ei se vor descompune în zeci de ani. Deocamdată să rămînem la cianura liberă din adîncime:
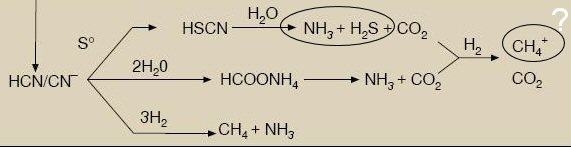
Pe ramura de sus este o nerealistă reacţie cu sulful nativ. Minereul de la Roşia nu conţine sulf nativ. Dar teoretic, cianura poate întîlni un ion de sulfură solubilă, care să reducă un ion metalic, apoi să formeze sulfocianură. Mult mai probabile sunt reacţiile de hidroliză a cianurii, cu dezaminare, la care se adaugă reacţii de reducere a sulfaţilor la sulfuri. Din cele două reacţii rezultă aceiaşi produşi încercuiţi pe ramura de sus: H2S şi NH3.
În schemă este şi o eroare ce a trecut neobservată din Australia în România, pînă aici în Japonia: am încercuit ionul CH4(+) deoarece e de fapt NH4(+) (ionul amoniu). Ar mai fi metanul. El ia naştere natural în mîluri, dar nu are sarcină electrică.
Hopa!
Combinaţia de hidrogen sulfurat cu amoniac este reactivul unei întregi grupe de analiză a cationilor, mai exact, grupa a III-a analitică, numită şi grupa sulfurii de amoniu. Puteţi reveni la lista de insolubile din articolul precedent, să observaţi că hidroxizii unor metale tranziţionale au produse de solubilitate foarte mici. De ordinul zece la puterea minus 18 – minus 36. Atît hidroxizii cît şi sulfurile lor precipită cantitativ.
Încet, încet, pe măsură ce hidrogenul sulfurat este fabricat de bacterii, el transformă pînă şi hidroxizii metalici în sulfuri.
O altă serie de reacţii va fi cea a smulgerii liganzilor din complecşii ciano-metalici sedimentaţi. Procesul va fi lung, deoarece necesită selectarea unor tulpini de bacterii în regim anaerob, rezistente la presiune. Hrana lor va consta chiar din carbonul şi azotul provenite din complecşii ciano-metalici. Se eliberează astfel ionii centrali, ce mai departe vor fi imobilizaţi sub formă de sulfuri.
Practic, în apele adînci are loc procesul invers, cel de întoarcere a metalelor toxice în stadiul anterior excavaţiei. Procesele reductive din mîlul apelor adînci sigilează practic ciclul: mobilizare-imobilizare.
Iazul nu va mirosi niciodată a hidrogen sulfurat, deoarece el va fi captat**) de ionii metalici.
Dacă ar fi să evaluăm, după mecanismele expuse mai sus, capacitatea de autoepurare a iazului, ea poate fi mai mică în primii ani, deoarece apele sunt mai puţin adînci, iar impurităţile din peisajul scufundat ar putea influenţa semnificativ pH-ul. Dar pe măsură ce sedimentele vor spori, inerţia sistemului va permite stabilizarea miocroflorei utile. Însă nu în tot cuprinsul. Cît timp vor fi deversate suspensii reziduale, va fi greu de menţinut un mediu favorabil productivităţii microbiologice. Oricum, exploatatorul va avea 16 ani la dispoziţie să amenajeze şi să optimizeze cele două lagune de epurare semipasivă din aval. Lagune despre care vom vorbi în următorul articol.
––––––––
*) sulfatul de calciu omniprezent în sediemnt face ca arseniaţii să devină complet insolubili. Pe acelaşi gen de reacţie, o instalaţie de defosforare (arsenul este rudă bună cu fosforul) a apelor reziduale din Hiroşima, foloseşte ca agent de defosforare spărturile panourilor de partiţionare a birourilor şi încăperilor. Aşadar, un deşeu de gips (sulfat de calciu) din construcţii este folosit pentru a preveni pătrunderea fosforului în mare, şi astfel a frîna dezvoltarea planctonului marin cu potenţial sufocant pentru culturile de stridii.
**) Într-un port din judeţul Yamaguchi, schimbul mareic de ape era insuficient pentru a împiedica dezvoltarea hidrogenului sulfurat în mîlul marin. Oamenii se plîngeau de miros. Soluţia a fost bascularea cîtorva tone de şpan de fier pe fundul portului. Fierul rugineşte, iar rugina captează hidrogenul sulfurat. Marea Neagră, de asemeni, se reîmprospătează o dată la 271 de ani (spre deosebire de Marea Mediterană, o dată la 80 de ani). Este cunoscută ridicarea uneori a hidrogenului sulfurat la suprafaţă. Fenomen ce le cam dă dureri de cap marinarilor.
★ Despre chimismul postminier la Roşia Montană (V)
În episodul trecut descoperirăm că o serie de reacţii de precipitare au loc chiar în tulbureala epuizată, în timpul fazei de detoxifiere a cianurilor. În altă parte am identificat cîteva antagonisme naturale ce se pot petrece chiar şi pe valea Roşia cum ar fi inocuizarea reciprocă a arsenului cu fierul. Problematică în inocuizarea naturală de pe valea Roşia este dezorganizarea terenului. Nu totdeauna se nimereşte combinaţia potrivită de ioni care să precipite şi astfel să devină netoxici.
Pe valea Corna, toate substanţele mai mult sau mai puţin toxice se adună în iaz, unde interacţiunile sunt mult mai libere şi în acelaşi timp mai bine izolate de vecinătăţile civile. Un ion metalic toxic, plecat din uzină, sau născut în iaz, are mult mai multe şanse de a-şi găsi perechea împreună cu care să precipite. Dacă nu la coada lacului, în orice altă parte a lui. Cu alte cuvinte, iazul de decantare este o mare haldă concavă, cu mare mobilitate internă. Observaţi diferenţa faţă de şiroirile dezordonate şi de ieşirile libere din sistem de pe valea Roşia. Pe scurt, iazul formează un sistem aproape închis, unde procesele chimice şi biochimice de inocuizare indusă sau naturală, au loc mai rapid şi mai bine controlat.
Desigur, există şi limite pe care vom încerca să le aflăm. Nu va fi prea uşor, dar nici imposibil.
Iată mai jos un tabel general de screening rapid. Puteţi imagina orice substanţă rezultată din datele de intrare, după care puteţi vedea rapid dacă este sau nu solubilă. Tabelul e preluat şi reformatat cu anionii pe linii şi cu cationii pe coloană. Este doar orientativ:

Pentru ceea ce ne interesează pe noi, am întocmit o listă cu produsele de solubilitate ale compuşilor pentru care am găsit date:
Arseniat de fier(3+) – FeAsO4 – 1.47xE-09%
Sulfocianură de plumb(2+) – Pb(SCN)2 – 0.553%
Hexacianoferat de mangan(2+) – Mn2Fe(CN)6 – 0.001882%
Hexacianoferat de plumb(2+) – PbFe(CN)6 – 0.0005991%
Sulfură de arsen (nativă) – As2S3 – 0.0004% (cca. 40mg/l)
Cianură de cadmiu – Cd(CN)2 – 0.022%
Hexacianoferat(II) de cadmiu – Cd2Fe(CN)6 – 0.00008736%
Carbonat de cadmiu – CdCO3 – 0.00003932%
Hidroxid de cadmiu – Cd(OH)2 – 7.2×E-15%
Molibdat de calciu – CaMoO4 – 0.004099%
Calcium phosphate – Ca3(PO4)2 – 0.002% (orientativ, pentru comparaţia cu arseniaţii)
Selenat de calciu – CaSeO4.2H2O – 9.22% (!)
Arseniat de cobalt(2+) Co3(AsO4)2 – 6.80×E-29mol/l
Sulfocianură de cupru(1+) – CuSCN – 8.427xE-07%
Sulfat de cobalt(2+) – CoSO4 – 36.1% (!)
Copper(I) cyanide CuCN 1.602E-09%
Hidroxid de cupru(2+) – Cu(OH)2 – 0.000001722%
Arseniat de cupru(2+) – Cu3(AsO4)2 -7.95×E-36mol/l
Oxalat de cupru – CuC2O4.2H2O – 2.1627xE-10%
Seleniat de cupru – CuSeO4 – 17.5% (!)
Selenit de cupru – CuSeO3 0.002761%
Seleniat de galiu(3+) – Ga2(SeO4)3.16H2O – 18.1% (!)
Hidroxid de galiu – Ga(OH)3 – 7.28×10-36mol/l
Hidroxid de indiu(3+) – In(OH)3 – 3.645xE-8%
Hidroxid de fier(2+) – Fe(OH)2 – 0.00005255%
Hidroxid de fier(3+) – Fe(OH)3 2.097xE-09%
Cromat de plumb(2+) – PbCrO4 – 0.0000171%
Hidroxid de plumb(2+) – Pb(OH)2 – 0.0001615%
Molibdat de plumb(2+) – PbMoO4 – 0.00001161%
Oxalat de plumb(2+) – PbC2O4 – 0.0006495%
Hidroxid de plumb(4+) – Pb(OH)4 – 7.229xE-11%
Sulfat de plumb (2+) – PbSO4 – 0.003836%
Seleniat de plumb(2+) – PbSeO4 – 1.37×10-7mol/l.
Ele pot fi mult mai multe. Le-am selectat pe cele cu solubilitate foarte scăzută, deoarece, ţinînd seama de pH-ul alcalin al apelor din iaz, formarea lor este mai probabilă.
Chiar dacă o sare solubilă se formează, fiind mediu apos, este imposibil ca anionul sau cationul să nu dea de un ion complementar cu care să precipite.
Din păcate nu am avut timp să unific unităţile de măsură. Unele substanţe sunt exprimate în moli la litru, altele, în procente. Valorile cu prea multe zerouri după virgulă sunt contrase ca puteri negative ale lui 10, exprimate ca „xE-8” de pildă, însemnînd că mantisa se împarte la 100 de milioane.
Deşi probabilitatea este mică, am listat şi cîţiva oxalaţi, ţinînd seama că dicianul este teoretic nitrilul acidului oxalic. În orice caz, formiaţii şi oxalaţii nu pot avea viaţă lungă într-un mediu în care foamea de substanţe organice este mare.
Am marcat cu semnul „(!)”, substanţe periculos de solubile, cărora nu le-am găsit un destin insolubil pe termen scurt. Este cazul seleniaţilor, care, deşi proporţional sunt în cantităţi infime, nu le-am întrevăzut reacţii de precipitare rapidă. Asta înseamnă că în apele iazului, se vor acumula seleniaţi şi posibil şi teluraţi.
Hopa!
Iată o oportunitate pentru Acad. Ionel Haiduc să propună o instalaţie de deseleniere a supernatantului din iaz, că tot plîngea după elementele valoroase. Ceva cu schimbători de ioni poate foarte bine concentra seleniul, cu costuri relativ mici.
Nu am pomenit nimic despre vanadiu şi titan. Nici nu e cazul. (Hidr)oxizii de vanadiu şi vanadaţii sunt de felul lor insolubili. Iar titanul nu va consimţi să se dizolve, în niciuna din fazele procesului tehnologic. Pentru vanadaţii şi polivanadaţii rezultaţi din oxidarea vanadiului din sulfuri, însuşi mineralul purtător de titan (probabil rutilul) reprezintă o matrice foarte bună de co-cristalizare. Afinitatea sterică reciprocă a oxizilor şi respectiv oxoanionilor celor două metale este foarte mare.
Aşadar, o mare parte din materiile toxice sunt, fie distruse, fie precipită. Dintre cele precipitate însă, rămîn periculoşi complecşii ciano-metalici, chiar dacă mai devreme sau mai tîrziu vor precipita stabil.
Hopa!
Acad. Ionel Haiduc semăna panica, bazîndu-se tocmai pe complecşii ciano-metalici. Spunea domnia-sa că la căldură se vor descompune volume uriaşe de feri- şi ferocianuri, otrăvind mediul. Date certe: la 70 de grade, fericianura abia începe să piardă apa de cristalizare. Iar de descompus, se descompune la fierbere. La altitudinea iazului, apa fierbe cam la 96 de grade. Va fi imposibilă descompunerea fericianurilor, chiar dacă întregul iaz ar fi aşezat pe o plită de 300ha.
Altfel, ferocianura de potasiu şi amoniu este folosită în zootehnie la doze de 1-15mg/kilocorp. Ceea ce înseamnă că un om de 70Kg poate înghiţi pînă la un gram de ferocianură, fără să se intoxice. Am găsit datele într-o documentaţie europeană datată 1998. Actul normativ este unul cu aplicare ocazională. Ferocianura solubilă este menită să prevină pătrunderea cesiului (radioactiv) în corpul animalului, în cazul unei catastrofe nucleare de pace. Ferocianura precipită cu cesiul, compus ce se elimină prin fecale, prevenind contaminarea internă. Aşadar, la concentraţiile mici de complecşi metalo-cianici, animalele din zonă nu ar suferi dacă ar bea accidental apă din iaz. Iar dacă unii complecşi ciano-metalici precipită cu ioni alcalini (cesiul este rudă cu sodiul şi cu potasiul) cu atît mai probabilă este precipitarea cu cationi metalelor tranziţionale.
Vom reveni la complecşii cianometalici atunci cînd vom vorbi despre chimismul pe termen lung.
★ Despre chimismul postminier la Roşia Montană (IV)
Facem întîi o scurtă incursiune în amplasament, pentru a ne fixa mai bine ceea ce este acid de ceea ce este alcalin.

În primplan este valea Roşia. Contururile portocalii indică cele patru cariere. (pentru persoanele mai impresionabile, cei „patru munţi” care sunt doi versanţi) Contururile galbene arată aproximativ unde vor fi halde de steril neprelucrat. Roca grosieră sterilă, se va folosi mai ales la astuparea carierelor Jig şi Orlea din partea dreaptă a văii (stînga în imagine). Apele scurse din cariere, sunt tributare, văii Roşia. Cele tehnologice, văii Corna. Apele acide vor fi numai pe valea Roşia (ca şi în prezent). Ele vor fi colectate într-un iaz mai mic, ce urmează a fi reconfigurat, de unde vor fi pompate în staţia de epurare de pe cumpăna celor două văi principale.
Pe valea Corna, cu albastru este marcat „iazul de cianuri”. (voi arăta mai tîrziu de ce între ghilimele.) În el se vor colecta şi niscai ape acide de pe haldele de steril grosier de pe versantul stîng.
Aşadar, valea Roşia va fi colectoare de ape acide, în timp ce valea Corna va colecta apele industriale alcaline şi va reţine şi sterilul măcinat, rezultat din procesul de extracţie-detoxifiere.
Organizarea spaţiului este mai detaliată în planul de amplasare din documentaţia RMGC:

Forma este de bumerang, cu braţele pe cele două văi. Se pot identifica cu verde ariile deneatins: stivele de sol vegetal, localităţi şi cartiere, aria protejată, monumente naturale şi cimitire. Vor mai fi două cariere, marcate cu roşu brun, una de andezit, în cotul bumerangului şi una de gresie, mai la vest, lîngă iazul de ape acide. Stiva de minereu sărac va fi chiar lîngă uzina de extracţie.
Să descriem sumar procesul de producţie. Minereul se macină fin, se amestecă cu var şi cu cianură şi se supune extracţiei. Adaosul de cărbune activ face ca metalele de interes să se concentreze în particulele de cărbune. După faza asta, partea electrochimică şi metalurgică nu ne interesează. Pentru noi, mai interesante sunt deşeurile.
Trebuie spus că la Baia Mare, tulbureala (minereu amestecat cu soluţii de chimicale) după ce se epuiza, cînd încă mai conţinea 500mg/l, se arunca direct în iaz. Altminteri, precar barat. Cumulul de nesimţiri a dus la accidentul din anul 2000.
Nu este cazul RM, unde norma internă de zvîrlire este de sub 3mg/l. Adică doar de 1/150 din ceea ce se petrecea la Baia Mare. Iar barajul va fi mai tare ca orice alt baraj de pe glob.
Cum ziceam, la Roşia Montană, partea interesantă pentru noi pe termen lung este tocmai ceea ce urmează la prelucrarea deşeurilor, deoarece, precum se ştie, în deşeuri rămîn şi cianuri nevolatile. De fapt, complecşi cianuraţi ai unor metale tranziţionale, a căror transformare ulterioară este de-a dreptul fascinantă.
Elementul cheie în tot procesul de inocuizare a deşeului este calciul. Este omniprezent. Încă de la faza de măcinare fină se adaugă var nestins. Cianura atacă sulfurile native şi eliberează anionul solubil sulfură S(2-). Prin dizolvarea piritelor ia naştere sulfura cel puţin parţială de calciu*) Ca(HS)2, care la rîndul ei, are puterea de a tăia punţile de sulf din pirite**) şi de a grăbi atacul.
Simultan, în băile de cianurare iau naştere şi tiocianaţii (numiţi şi sulfocianuri sau rodanuri) cu care încerca acad. Ionel Haiduc să sperie lumea. Tiocianaţii, la fel ca cianaţii tipici (cianuri cu oxigen în moleculă) sunt compuşi metastabili. Procedeul detox cu dioxid de sulf şi oxigen, catalizat cu ioni de cupru, face praf cam tot ce e tiocianat. Oxidarea are loc asemănător cu cea din suveica de fier(3+)-fier(2+), descrisă anterior. Cuprul divalent oxidează sulfocianura şi în acelaşi timp se reduce la cupru monovalent, ce ulterior este din nou oxidat în mediul puternic oxigenat, la cupru divalent. Iată curba destrucţiei sulfocianurilor în timp:
În mai puţin de 30′, sulfocianura se duce naibii. Presupunînd că nu se duce naibii cu totul, ea este toxică în proporţie de doar 1/7 din cea a cianurilor solubile, deoarece cam toate vietăţile moştenesc gene ce fac posibilă sinteza unei enzime numite rodanază, responsabilă de detoxifierea intracelulară a sulfocianurilor. Moştenirea ne vine de pe vremea cînd atmosfera Pămîntului conţinea acid cianhidric şi era reducătoare.
Hopa!
Dacă vreţi să vă convingeţi de prezenţa sau de absenţa sulfocianurilor în iaz, într-o excursie de documentare puteţi lua o sticluţă cu soluţie diluată de clorură ferică. Dacă la amestecarea apei din iaz cu clorura ferică, conţinutul flaconuluise înroşeşte, înseamnă că încă mai sunt tiocianaţi liberi. Puţin probabil. Voi arăta şi mai jos, şi în altă parte, de ce.
Ţinînd seama de rolul cheie al ionilor de cupru în catalizarea destrucţiei toxicelor, cine a pus la punct tehnologia nu s-a bazat nici măcar pe cuprul nativ prezent în minereu. Lista de chimicale cuprinde cîteva sute de tone de piatră vînătă, ce se adaugă în procesul detox. Semnul că exploatatorul nu îşi permite să se facă doar că detoxifică.
Conform procedeului de extracţie descris în raportul de mediu, cianura liberă din tulbureală, se recirculă parţial, ceea ce reduce volumul suspensiei de tratat. De asemeni, conţinutul de cianuri din faza apoasă scade încă din prima etapă a extracţiei, datorită complexării cu ionii metalelor tranziţionale din sistem şi a conversiei cianurilor în tiocianaţi. La detoxifierea accelerată, în atmosferă de dioxid de sulf şi oxigen, alte procese favorabile se petrec: sulfaţii formaţi reduc pH-ul, dar în acelaşi timp, ionii de amoniu rezultaţi din una din reacţiile de oxidare a cianurii, îl ridică. Amoniacul, împreună cu hidrogenul sulfurat provenit din hidroliza parţială a sulfurilor solubile, au darul să precipite din nou metalele tranziţionale, fie sub formă de hidroxizi, fie direct sub formă de sulfuri.
Hopa!
Reţineţi alăturarea: H2S şi NH3, deoarece ne vom mai întîlni cu ea în iaz, în cu totul alte împrejurări.
Desigur, tiocianaţii mai au marele avantaj că, odată oxidaţi, devin radicali liberi, puternic reactivi, ce dau startul unei game largi de reacţii de oxidare atît a dioxidului de sulf şi a sulfurilor, cît şi a ionului, cian, direct în dioxid de carbon şi azot. Două gaze neotrăvitoare, din care unul are darul să precipite suplimentar ionii metalelor tranziţionale şi calciul, la carbonaţi. Excesul de ioni sulfat şi sulfit sunt însă fixaţi în faza solidă tot de către calciu.
După cum vedem, multe reacţii de precipitare au loc chiar în timpul procesului de extracţie şi detoxifiere. Ele pot continua şi se diversifică în iaz, în măsura în care încă se mai află metalice toxice în soluţie.
Într-un post viitor voi privi critic reacţiile chimice şi biochimice din ramura de inocuizare pe termen lung (valea Corna). Tot atunci voi schiţa şi un mic bilanţ de materiale pentru metalele toxice. Voi spune două vorbe şi despre extincţia lor în timp.
––––––-
*) sulfurile alcalino-pămîntoase au proprietatea de a rupe punţile de sulf din proteine, făcîndu-le solubile. Aşa de pildă, sulfura de bariu este folosită la epilarea cobailor, atunci cînd sunt folosiţi ca hrană pentru ţînţarii de experienţă. Pentru uz uman se folosesc compuşi organici (acid tioglocolic, ditiothreitol etc.), dar cam tot pe acelaşi mecanism acţionează.
**) în pirite, compuşi naturali, starea de oxidare a sulfului nu este întotdeauna (2-) ci adesea este (1-), prin combinarea sulfului cu el însuşi. Cum sulful este rudă cu oxigenul, piritele pot fi considerate omologii peroxizilor, substanţe instabile, în care oxigenul se leagă de el însuşi.
★ Despre chimismul postminier la Roşia Montană (I)
Articolul de faţă se adresează oamenilor raţionali cu oarece cunoştinţe de chimie, dar nu prea multe.
Studiind datele despre sursele de apă monitorizate pe durata a 10 ani de către RMGC, am observat că practic compoziţia lor chimică diferă atît în spaţiu cît şi în timp. Practic nu există o corelaţie certă între anotimpul, originea, regimul pluvial şi natura rocilor. Singurul parametru cu oarece legătură este pH-ul. Cu cît mai acid, cu atît mai mare mineralizaţia apelor.
Să trecem aşadar la problema propriu-zisă. Întrebarea este: de unde vine poluarea cu metale?
Răspunsul simplu este: din alterarea rocilor.
Cum?
În zăcămînt sunt cam patru feluri mari de roci, constituite din sute de minerale şi minerăluţe. La contactul cu oxigenul cu apa şi cu lumina, mineralele încep să se transforme. Unele se dizolvă, altele dau produşi tot insolubili. Nu e greu să ne dăm seama că suprafaţa de contact cu mediul, cu cît este mai mare, cu atît mai intensă va fi alterarea. De asemeni, cu cît durata de contact cu aceeaşi cantitate de solvent e mai mare, cu atît mai concentrată va ieşi soluţia de poluanţi. Prezenţa unora dintre microorganismele ce metabolizează metale este de asemeni importantă în calitatea outputului.
Aria de contact
La ora actuală, aria totală de contact este imposibil de estimat. Se pot face doar estimări macroscopice. Avem 22 de halde vechi, ce nu par a fi în vreun fel compactate, dar se întind pe zeci de hectare. Nu e greu să ne dăm seama că cu cît sunt mai mărunţite şi mai afînate, cu atît sunt mai generoase în poluanţi. Afînarea haldelor şi a rambleurilor înzeceşte aria expusă. Se adaugă eroziunea ce, prin ravenele de şiroire multiplică suprafaţa totală de contact.
Mai există două cratere, din care unul rambleiat. Alte zeci de hectare de rocă expusă degradării. Iar craterul Cetate pare a avea şi drenaj, ceea ce asigură scurgerea nestînjenită a poluanţilor în valea Roşia.
Mai sunt 140Km de galerii, din care au fost scoase de-a lungul vremii peste 2 megatone de rocă. Dacă socotim diametrul mediu de 4 metri*) rezultă alte 176ha de rocă expusă degradării, chiar dacă nu la vedere. (spre comparaţie, perimetrul minier nu are mai mult de 1200ha, din care jumătate nu va avea roca expusă.)
Durata de staţionare a apei
Intuitiv, ne dăm seama că băltirea duce la concentraţii mai mari de poluanţi Iar de băltire avem parte în toate cele trei forme de degradare: în galerii, în halde, în cratere. De reţinut că cu cît panta este mai mică, cu atît băltirea are o pondere mai mare. Dintre toate formele de acumulare şi deversare a apei băltinde, cea mai imprevizibilă este cea din subteran. Nu numai prin duratele mari de staţionare, dar şi prin fenomene accidentale de sifonare din galeriile părăsite. Cine ştie cîte ceva despre carstul subteran, ştie că sifoanele pot lua naştere natural. O galerie sinuoasă pe verticală, se poate umple, iar la un moment dat, sifonul se amorsează şi deversează mii de metri cubi de apă „stătută” printr-un izbuc pulsativ. Conformaţiile cu potenţial de sifonare nu sunt imposibile atunci cînd ai 140Km de galerii. Iar emergenţa aleatorie din galerii poate fi o explicaţie pentru compoziţia atît de capricioasă a apelor de mină în timp.
Am văzut aşadar cam cît de mare este aria rocilor supuse alterării naturale. Sunt mii de hectare macroscopice şi alte zeci de mii microscopice. La haldele de steril rezultat din flotaţie, aria unui metru cub poate depăşi şi 5ha. Şi sunt milioane de metri cubi. Din fericire, haldele se mai compactează şi natural, ceea ce scade mult aria specifică.
Am descris situaţia prezentă.
Ce e de făcut?
Nu e greu de intuit că distrugerea sistemului de galerii prin detonare reduce mult aria de expunere a rocii la alterare. Craterele rezultate au oricum aria limitată, iar durata de expunere la degradare are un gradient vertical. Mai mare sus, mai mică jos. Aria ce sporeşte prin adîncire, este compensată atît de reducerea ariei galeriilor cît şi de drenajul mai uşor de controlat. Haldele oricum vor fi compactate şi împrejmuite de şanţuri de drenaj, ceea ce reduce mult şi din aria de expunere microscopică. Sterilele colectate în iazul de decantare vor avea aria de expunere de maximum 363ha. Iar aria microscopică redusă doar la atît cît permite oglinda de apă. Adică, doar pe la coada iazului.
Avantajul iazului de decantare este evident. Nu numai că asigură recircularea apei, dar, prin pH-ul său alcalin, dă naştere unui chimism diferit de cel de pe valea Roşia. (voi detalia într-un articol viitor.) Nu greşim dacă considerăm sedimentele de acolo ca fiind o mare haldă întoarsă cu fundul în sus şi complet compactată. Mai mult, iazul de pe Corna poate fi folosit ca receptor şi neutralizator grosier de ape acide provenite de pe valea Roşia, datorită pH-ului ridicat, mai ales în situaţii de urgenţă (ruperi de nori).
De unde vine alcalinitatea iazului? Din megatona de var nestins ce va fi folosit la tratarea minereului.
Aşadar, pentru apele acide de pe valea Roşia să fie tratate, este nevoie a fi drenate într-un singur iaz de colectare. Doar acolo ele vor avea o compoziţie cît de cît previzibilă în timp. Cît timp RMGC le va exploata pentru extracţia aurului, apele acide vor înceta să mai polueze Abrudul şi Arieşul.
După încheierea proiectului minier, configuraţia terenului, reducerea ariei de alterare a rocilor va face mult mai simplă gestionarea scurgerilor. Iazul de ape acide va fi parte dintr-un sistem mai complex de captare şi epurare pentru uz casnic, industrial şi de salubrizare a cîtorva cursuri naturale de apă.
Aşadar, visul ecologiştilor de curăţenie va fi îndeplinit. Şi încă rapid. Nu însă fără efort. Efort pe care nu trebuie să îl facă ei. Îl va face exploatatorul. După încheierea proiectului, doar vrednicia primăriei, adică a aleşilor locali, va face diferenţa dintre bine şi rău.
Iată că nu am apucat să vorbesc despre chimism, ci despre lucruri mult mai simple. Am mutat şi discuţia despre microorganisme acolo, deoarece ea are aface mai mult cu chimismul intim decît cu aspectele ochiometrice şi de peisaj.
–––––––
*) în realitate sunt galerii înguste alternînd cu galerii largi şi cu domuri şi mai largi.

 Alin Fumurescu
Alin Fumurescu
12 comments